Ligações Químicas:
Os átomos dificilmente ficam sozinhos na natureza. Eles tendem a se unir uns aos outros, formando assim tudo o que existe hoje.
Alguns átomos são estáveis, ou seja, pouco reativos. Já outros não podem ficar isolados. Precisam se ligar a outros elementos. As forças que mantêm os átomos unidos são fundamentalmente de natureza elétrica e são chamadas de Ligações Químicas.
Há três tipos de ligações químicas:
Alguns átomos são estáveis, ou seja, pouco reativos. Já outros não podem ficar isolados. Precisam se ligar a outros elementos. As forças que mantêm os átomos unidos são fundamentalmente de natureza elétrica e são chamadas de Ligações Químicas.
Há três tipos de ligações químicas:
- Ligação Iônica – perda ou ganho de elétrons.
- Ligação Covalente – compartilhamento de elétrons.
- Ligação Metálica – átomos neutros e cátions mergulhados numa "nuvem" de elétrons.
Ligações Iônicas:
A ligação iônica é resultado da alteração entre íons de cargas elétricas contrárias (ânions e cátions).
Esta ligação acontece, geralmente, entre os metais e não-metais.
Metais – 1 a 3 elétrons na última camada; tendência a perder elétrons e formar cátions. Elementos mais eletropositivos ou menos eletronegativos.
Não-Metais – 5 a 7 elétrons na última camada; tendência a ganhar elétrons e formar ânions. Elementos mais eletronegativos ou menos eletropositivos.
Então:
METAL + NÃO-METAL → LIGAÇÃO IÔNICA
Exemplo: Na(Sódio) e Cl(cloro)
Na (Z = 11) → K = 2 L = 8 M = 1
Cl (Z = 17) → K = 2 L = 8 M = 7
O Na quer doar 1 é → Na + (cátion)
O Cl quer receber 1 é → Cl – (ânion)
O cloro quer receber 7é na última camada. Para ficar com 8é (igual aos gases nobres) precisa de 1é.
Na+ Cl – → NaCl
cátion ânion cloreto de sódio
As ligações iônicas formam compostos iônicos que são constituídos de cátions e ânions. Tais compostos iônicos formam-se de acordo com a capacidade de cada átomo de ganhar ou perder elétrons. Essa capacidade é a valência.
Exemplo: Mg e Cl
Mg+² Cl-¹ → MgCl2
cátion ânion cloreto de magnésio
Pode-se utilizar a “Regra da Tesoura”, onde o cátion passará a ser o número de cloros (não-metal) na fórmula final e o ânion será o número de magnésio (metal).
Esta ligação acontece, geralmente, entre os metais e não-metais.
Metais – 1 a 3 elétrons na última camada; tendência a perder elétrons e formar cátions. Elementos mais eletropositivos ou menos eletronegativos.
Não-Metais – 5 a 7 elétrons na última camada; tendência a ganhar elétrons e formar ânions. Elementos mais eletronegativos ou menos eletropositivos.
Então:
METAL + NÃO-METAL → LIGAÇÃO IÔNICA
Exemplo: Na(Sódio) e Cl(cloro)
Na (Z = 11) → K = 2 L = 8 M = 1
Cl (Z = 17) → K = 2 L = 8 M = 7
O Na quer doar 1 é → Na + (cátion)
O Cl quer receber 1 é → Cl – (ânion)
O cloro quer receber 7é na última camada. Para ficar com 8é (igual aos gases nobres) precisa de 1é.
Na+ Cl – → NaCl
cátion ânion cloreto de sódio
As ligações iônicas formam compostos iônicos que são constituídos de cátions e ânions. Tais compostos iônicos formam-se de acordo com a capacidade de cada átomo de ganhar ou perder elétrons. Essa capacidade é a valência.
Exemplo: Mg e Cl
Mg+² Cl-¹ → MgCl2
cátion ânion cloreto de magnésio
Pode-se utilizar a “Regra da Tesoura”, onde o cátion passará a ser o número de cloros (não-metal) na fórmula final e o ânion será o número de magnésio (metal).
Ligações Covalentes:
A ligação covalente, geralmente é feita entre os não-metais e não-metais, hidrogênio e não-metais e hidrogênio com hidrogênio.
Esta ligação é caracterizada pelo compartilhamento de elétrons. O hidrogênio possui um elétron na sua camada de valência. Para ficar idêntico ao gás nobre hélio com 2 elétrons na última camada. Ele precisa de mais um elétron. Então, 2 átomos de hidrogênio compartilham seus elétrons ficando estáveis:
Ex. H (Z = 1) K = 1
H – H → H2
O traço representa o par de elétrons compartilhados.
Nessa situação, tudo se passa como se cada átomo tivesse 2 elétrons em sua eletrosfera. Os elétrons pertencem ao mesmo tempo, aos dois átomos, ou seja, os dois átomos compartilham os 2 elétrons. A menor porção de uma substância resultante de ligação covalente é chamada de molécula. Então o H2 é uma molécula ou um composto molecular. Um composto é considerado composto molecular ou molécula quando possui apenas ligações covalentes.
Conforme o número de elétrons que os átomos compartilham, eles podem ser mono, bi, tri ou tetravalentes.
A ligação covalente pode ocorrer também, entre átomos de diferentes elementos, por exemplo, a água.
Observe a ligação covalente entre dois átomos de cloro:
Cl – Cl Cl 2
Fórmula Estrutural Fórmula Molecular
Esta ligação é caracterizada pelo compartilhamento de elétrons. O hidrogênio possui um elétron na sua camada de valência. Para ficar idêntico ao gás nobre hélio com 2 elétrons na última camada. Ele precisa de mais um elétron. Então, 2 átomos de hidrogênio compartilham seus elétrons ficando estáveis:
Ex. H (Z = 1) K = 1
H – H → H2
O traço representa o par de elétrons compartilhados.
Nessa situação, tudo se passa como se cada átomo tivesse 2 elétrons em sua eletrosfera. Os elétrons pertencem ao mesmo tempo, aos dois átomos, ou seja, os dois átomos compartilham os 2 elétrons. A menor porção de uma substância resultante de ligação covalente é chamada de molécula. Então o H2 é uma molécula ou um composto molecular. Um composto é considerado composto molecular ou molécula quando possui apenas ligações covalentes.
Conforme o número de elétrons que os átomos compartilham, eles podem ser mono, bi, tri ou tetravalentes.
A ligação covalente pode ocorrer também, entre átomos de diferentes elementos, por exemplo, a água.
Observe a ligação covalente entre dois átomos de cloro:
Cl – Cl Cl 2
Fórmula Estrutural Fórmula Molecular
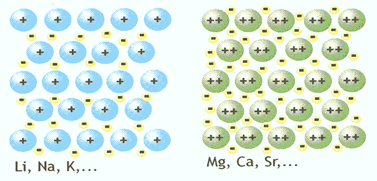
Ligações Metálicas:
Tomamos contato diário com muitas substâncias formadas apenas por átomos de metais, chamadas substâncias metálicas. Entre os exemplos mais conhecidos estão o ferro, o alumínio, o chumbo, o cobre e a prata.
Como os átomos se unem para formar essas substâncias?
Vamos olhar para o modelo do átomo abaixo. Os elétrons, dotados de carga negativa, são atraídos pelo núcleo, no qual, além dos nêutrons, estão os prótons, que apresentam carga positiva. A atração que o núcleo, carregado positivamente, exerce sobre os elétrons é responsável pelo fato de esses elétrons permanecerem no átomo, em vez de o abandonarem.
Uma idéia semelhante a essa pode ser usada para imaginar a ligação entre átomos de metais, denominada ligação metálica.
Como os átomos se unem para formar essas substâncias?
Vamos olhar para o modelo do átomo abaixo. Os elétrons, dotados de carga negativa, são atraídos pelo núcleo, no qual, além dos nêutrons, estão os prótons, que apresentam carga positiva. A atração que o núcleo, carregado positivamente, exerce sobre os elétrons é responsável pelo fato de esses elétrons permanecerem no átomo, em vez de o abandonarem.
Uma idéia semelhante a essa pode ser usada para imaginar a ligação entre átomos de metais, denominada ligação metálica.
Consideremos uma amostra da substância simples prata. Ela é formada por um aglomerado de muitos átomos de elemento químico prata. Nesse aglomerado, cada átomo está rodeado por outros átomos iguais a ele. O núcleo de cada átomo exerce atração sobre os elétrons de sua eletrosfera e também sobre os elétrons dos átomos vizinhos, mantendo toda a estrutura unida.
Os elétrons, por sua vez, não estão totalmente presos a um átomo apenas, podendo “transitar” por toda a estrutura. Alguns cientistas usam a expressão “mar de elétrons” para designar essa situação.
As substâncias metálicas (ou, simplesmente, metais) são úteis ao ser humano devido às suas propriedades, que, de modo bem genérico, são as listadas a seguir:
Os elétrons, por sua vez, não estão totalmente presos a um átomo apenas, podendo “transitar” por toda a estrutura. Alguns cientistas usam a expressão “mar de elétrons” para designar essa situação.
As substâncias metálicas (ou, simplesmente, metais) são úteis ao ser humano devido às suas propriedades, que, de modo bem genérico, são as listadas a seguir:
- Brilho característico. Quando polidos, os metais refletem muito bem a luz. Essa propriedade é fácil de ver em bandejas e espelho de prata.
- Alta condutividade térmica e elétrica. São propriedades que se devem aos elétrons livres. O movimento ordenado dos elétrons constitui a corrente elétrica e sua agitação permite a rápida programação do calor através das substâncias metálicas.
- Altos pontos de fusão e ebulição. Em geral são características dos metais (embora, haja exceções, como mercúrio, PF = -39ºC; gálio, PF = 30ºC, e potássio, PF = 63ºC). Devido a essa propriedade e também à boa condutividade térmica, alguns metais são usados em panelas e em radiadores de automóveis.
- Maleabilidade. Metais são muito maleáveis, ou seja, fáceis de serem transformados em lâminas. O metal mais maleável é o ouro, que permite a obtenção das lâminas mais finas.
- Ductibilidade. Metais também são muito dúcteis, isto é, fáceis de serem transformados em fios. O ouro é também o mais dúctil dos metais, permitindo que dele se obtenham fios finíssimos.